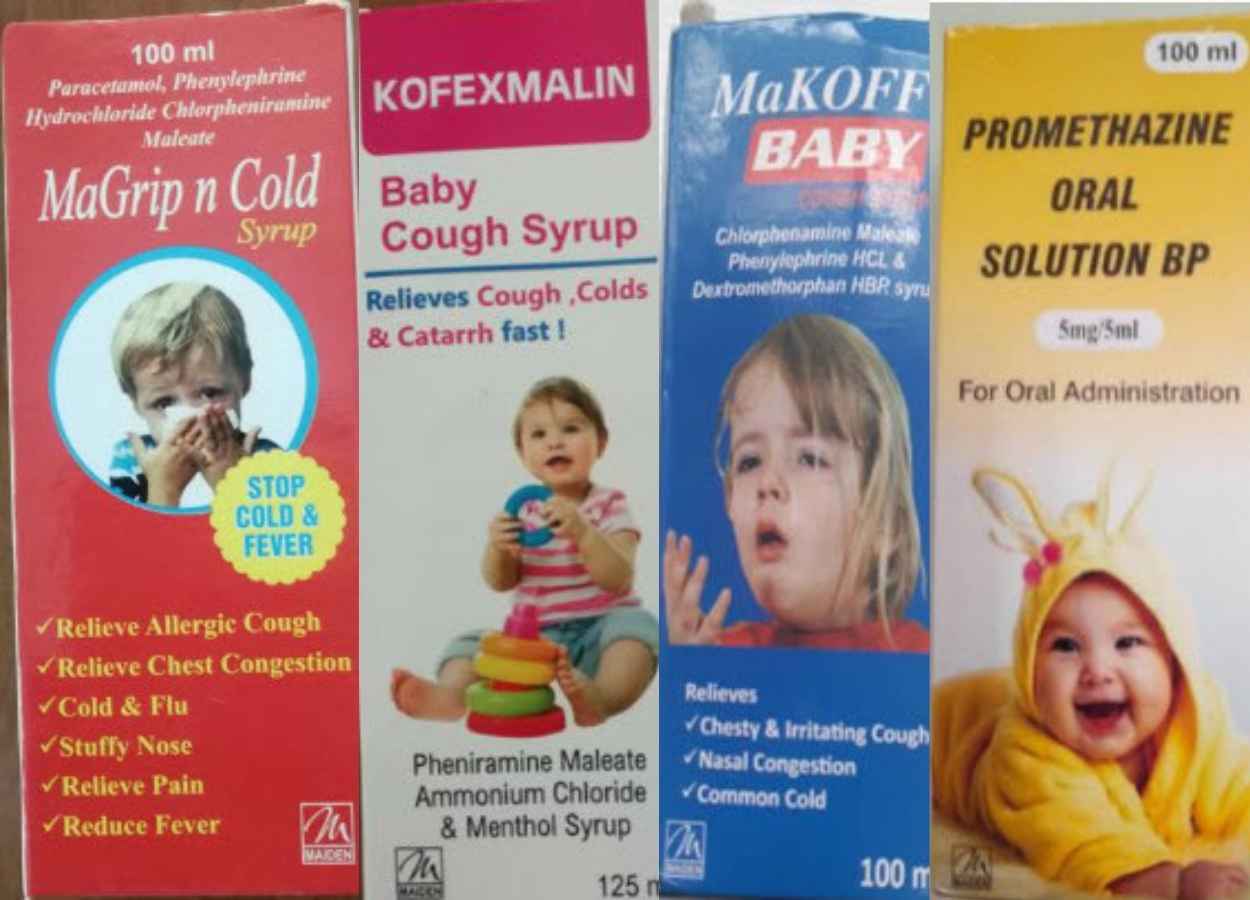
JAKARTA – Badan Pengawas Obatan dan Makanan (BPOM) kembali menegaskan bahwa obat sirup untuk anak yang disebutkan dalam informasi dari WHO, terdiri dari Promethazine Oral Solution, Kofexmalin Baby Cough Syrup, Makoff Baby Cough Syrup, dan Magrip N Cold Syrup. Keempat produk tersebut diproduksi oleh Maiden Pharmaceuticals Limited, India.
Dia juga menyebutkan keempat produk yang ditarik di Gambia tersebut tidak terdaftar dan tidak beredar di Indonesia dan hingga saat ini, produk dari produsen Maiden Pharmaceutical Ltd, India tidak ada yang terdaftar di BPOM.
“BPOM melakukan pengawasan secara komprehensif pre- dan post-market terhadap produk obat yang beredar di Indonesia. Sesuai dengan peraturan dan persyaratan registrasi produk obat, BPOM telah menetapkan persyaratan bahwa semua produk obat sirup untuk anak maupun dewasa, tidak diperbolehkan menggunakan EG dan DEG,” ujarnya dalam keterangan resminya di Jakarta, Rabu (20/10/2022)
Namun demikian, kata dia, EG dan DEG dapat ditemukan sebagai cemaran pada gliserin atau propilen glikol yang digunakan sebagai zat pelarut tambahan, BPOM telah menetapkan batas maksimal EG dan DEG pada kedua bahan tambahan tersebut sesuai standar internasional.
Sebelumnya, Kementerian Kesehatan (Kemenkes) telah menjelaskan bahwa penyebab terjadinya gagal ginjal akut atau Acute Kidney Injury (AKI) belum diketahui dan masih memerlukan investigasi lebih lanjut bersama BPOM, Ikatan Dokter Anak Indonesia (IDAI), dan pihak terkait lainnya.
BPOM mendorong tenaga kesehatan dan industri farmasi untuk aktif melaporkan efek samping obat atau kejadian tidak diinginkan pasca penggunaan obat sebagai bagian dari pencegahan kejadian tidak diinginkan yang lebih besar dampaknya.
“Diketahui BPOM juga berkoordinasi secara intensif dengan Kementerian Kesehatan, sarana pelayanan kesehatan, dan pihak terkait lainnya dalam rangka pengawasan keamanan obat (farmakovigilans) yang beredar dan digunakan untuk pengobatan di Indonesia,” ucapnya
Dia mengatakan BPOM juga melakukan penelusuran berbasis risiko, sampling, dan pengujian sampel secara bertahap terhadap produk obat sirup yang berpotensi mengandung cemaran EG dan DEG.
“Hasil pengujian produk yang mengandung cemaran EG dan DEG tersebut masih memerlukan pengkajian lebih lanjut untuk memastikan pemenuhan ambang batas aman berdasarkan referensi,” terang dia
Selanjutnya, kata dia untuk produk yang melebihi ambang batas aman akan segera diberikan sanksi administratif berupa peringatan, peringatan keras, penghentian sementara kegiatan pembuatan obat, pembekuan sertifikat Cara Pembuatan Obat yang Baik (CPOB), pencabutan sertifikat CPOB, dan penghentian sementara kegiatan iklan, serta pembekuan Izin Edar dan/atau pencabutan Izin Edar.
“Semua industri farmasi yang memiliki obat sirup yang berpotensi mengandung cemaran EG dan DEG, diminta untuk melaporkan hasil pengujian yang dilakukan secara mandiri sebagai bentuk tanggung jawab pelaku usaha. Industri farmasi juga dapat melakukan upaya lain seperti mengganti formula obat dan/atau bahan baku jika diperlukan,” pungkasnya.
Jurnalis: Agung Nugroho











Tinggalkan Balasan